A terapia de quelação é o principal processo para tratar intoxicação por metais pesados. Nesse processo, um ligante multidentado se liga a um íon metálico por mais de um átomo ligante em uma reação ácido-base onde o íon metálico é o ácido de Lewis (aceita par de elétrons) e o ligante é a base de Lewis (doa par de elétrons).
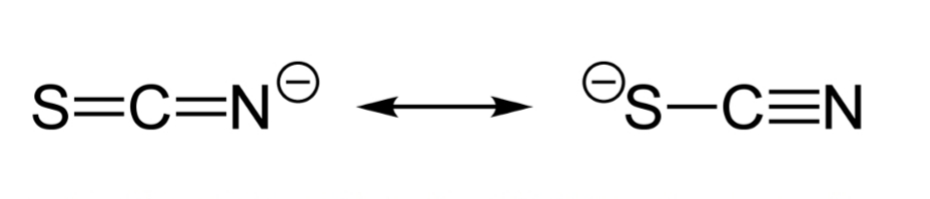
Na química de coordenação, existe uma classificação para os tipos de ligantes, eles podem ser classificados como monodentados, ou seja, que possuem um átomo doador de par de elétrons (por exemplo: Cl–, NH3 e H2O), bidentados com dois átomos doadores, por exemplo o ânion oxalato (C2O42-), multidentados com mais de dois átomos doadores, como por exemplo o ácido etilenodiamino tetra-acético (EDTA) ou ambidentados, que se ligam com um átomo central através de dois átomos diferentes como por exemplo o ânion tiocianato (SCN–). Os ligantes multidentados formam complexos com anéis de cinco a seis membros, o que os tornam mais estáveis que os ligantes monodentados, entretanto, a estabilidade desses complexos pode variar com interação metal-ligante.
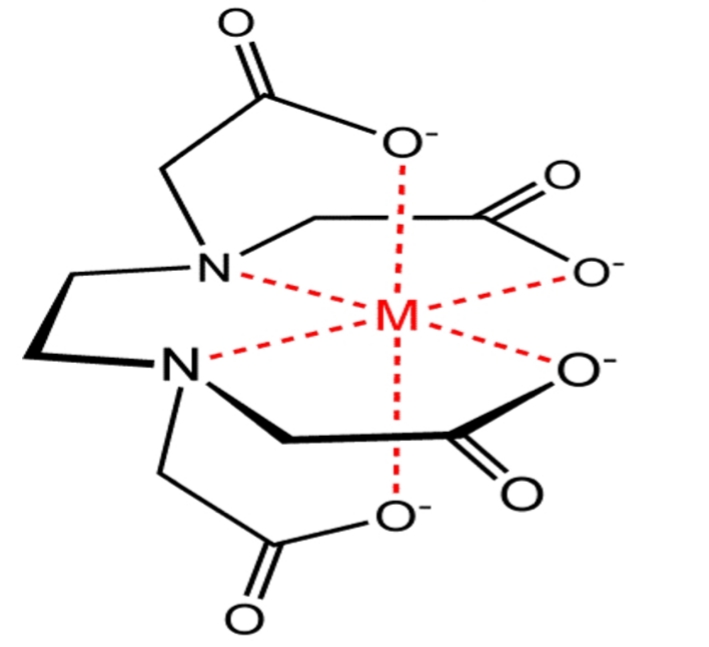
Figura 1: complexação de um metal por EDTA
Figura 2: ligante ambidentado (tiocianato)
Um bom agente quelante é caracterizado por formar complexos inertes e com baixa toxicidade. Além disso, podem ser administrados por via oral, intravenosa ou intramuscular e são excretados do organismo sem qualquer interação adicional com órgãos vitais. Eles também possuem a capacidade de adentrar na membrana celular para complexar metais tóxicos intracelulares. Outra característica é que um bom agente quelante tem uma afinidade maior por metais mais tóxicos do que pelos metais corporais e pode competir com ligantes endógenos (que são formados no próprio organismo).
Metais pesados são metais que possuem densidade maior que 5g/cm3 e são divididos em dois grupos, os essenciais e os não-essenciais. Os essenciais são inofensivos em baixas concentrações como (Zn, Co, Cu e Fe), já os não-essenciais são perigosos para a saúde humana devido sua elevada toxicidade como (Cd, Hg, As e Cr).
O envenenamento por metais pesados é mais comum em indivíduos que tem contato frequente com atividades de mineração, industriais, agrícola, fundição, esgoto e consumo excessivo de alguns alimentos como peixes pode desencadear uma intoxicação por metilmercúrio (H3C- Hg+).
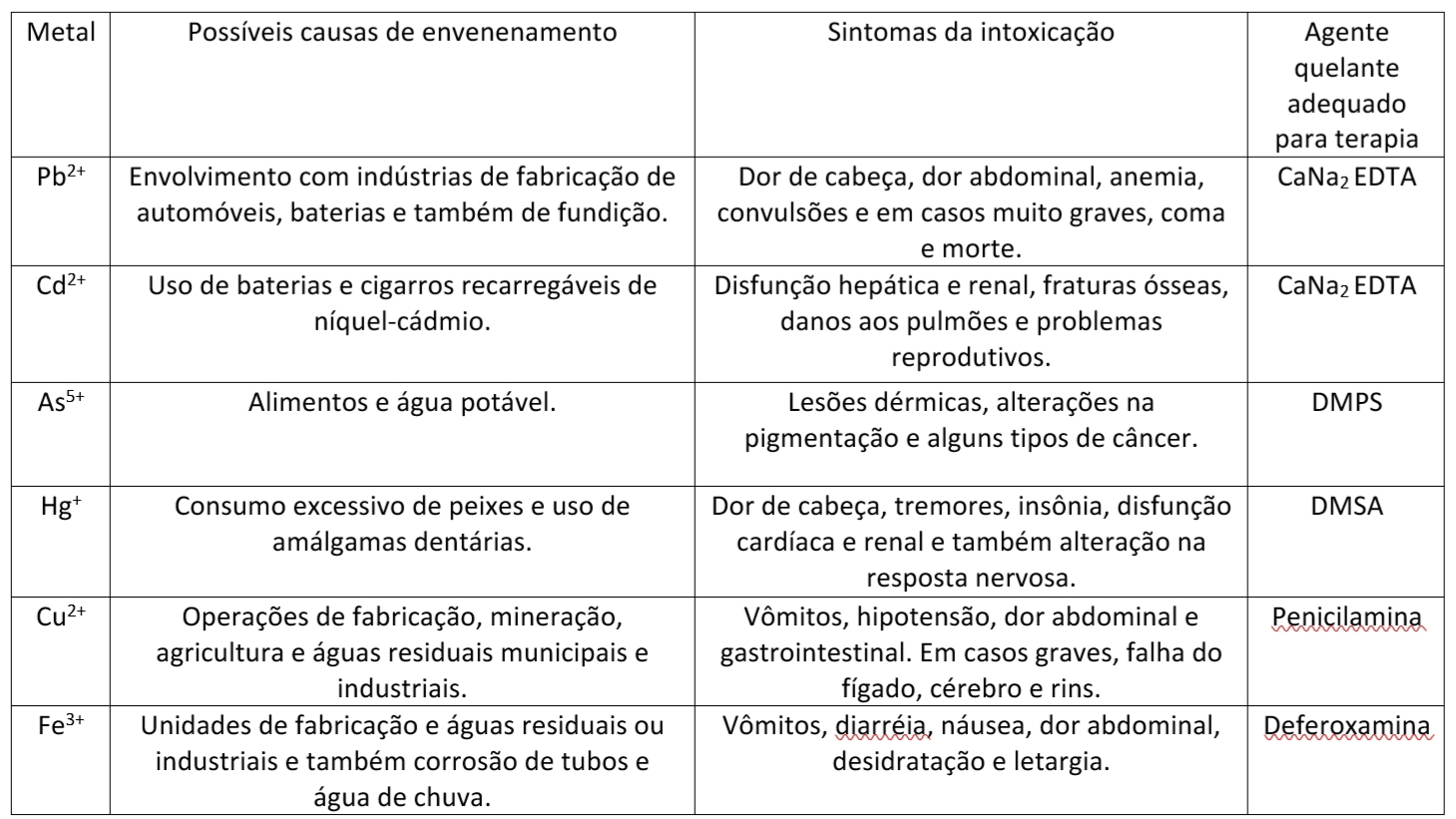
Os principais metais pesados que podem causar intoxicação são o chumbo (Pb2+), cádmio (Cd2+), ferro (Fe3+), arsênico (As5+), mercúrio (Hg+) e cobre (Cu2+).
Os principais agentes quelantes utilizados para complexar os metais citados acima são:
– CaNa2 EDTA (Edetato dissódico de cálcio)
– Dimercrapol (2,3- dimercaptopropanol)
– Penicilamina (Ácido (2S) -2-amino-3-metil-3-sulfanil-butanóico)
– DMSA (Ácido dimercaptosuccínico)
– DFO (Deferoxamina)
– miADMSA (Ácido monoisoamil-2,3-dimercaptosuccínico)
– DMPS (3-dimercapto-propanossulfato)
Tabela 1
A terapia por quelação é eficiente e é protocolo padrão para casos de intoxicação por metais pesados, entretanto, também há seus efeitos colaterais, dentre eles estão a febre, problemas de pressão, náusea, dor muscular e gastrointestinal. As doses do agente quelante deve ser rigorosamente controlada para evitar a perda de metais essenciais do organismo e também para evitar a intoxicação pelo próprio agente quelante que em doses elevadas pode piorar a condição do paciente. Além de ressaltar que o agente deve ter uma boa afinidade com o metal de interesse.
Bibliografia:
MIESSLER, G.; FISCHER, P. J.; TARR, D. A. Química Inorgânica. 5ª ed. São Paulo: Pearson Education, 2014.
KIM, J. J., KIM, Y. S., & KUMAR, V. (2019). Heavy metal toxicity: An update of chelating therapeutic strategies. Journal of Trace Elements in Medicine and Biology, 54(May), 226–231. https://doi.org/10.1016/j.jtemb.2019.05.003
HARRIS, Daniel C.; BONAPACE, José Alberto Portela; BARCIA, Oswaldo Esteves. Análise química quantitativa. 8. ed. Rio de Janeiro: LTC, 2012.