O hidróxido de sódio é um sólido branco higroscópico (absorve humidade do ambiente), solúvel em água que se comporta como base de Arrhenius. No mercado, sua aquisição pode ser feita em forma de escamas, pó, lentilhas, pérolas e micropérolas. Por possuir uma ampla utilização na indústria como na fabricação de papel, alumina, sabões, e síntese de fármacos, existe uma grande demanda do reagente. Por esse motivo, diversos métodos são usados para a sua fabricação, dentre eles destacam-se a célula de Mercúrio, a célula de membrana e a célula de diafragma.
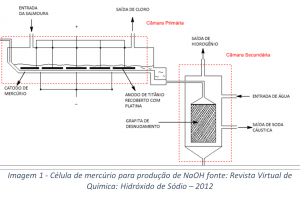
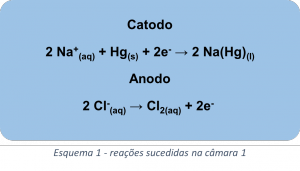
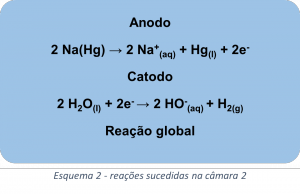
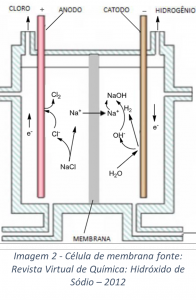
O método da célula de Mercúrio envolve a utilização de duas câmaras, a câmara primária é composta por catodos de mercúrio e anodos de titânio recobertos de platina (Imagem 1). Inicialmente a câmara primária é abastecida com uma solução concentrada de NaCl, em seguida o cátion sódio sofre redução no catodo onde se deposita na forma de sódio metálico (Na), e se dissolve no mercúrio formando amálgama de sódio Na(Hg), observe a equação química no esquema 1. Enquanto isso, nos anodos de titânio recobertos por platina, o íon cloro sofre oxidação transformando-se em cloro gasoso que é imediatamente liberado, observe a equação química do esquema 1. Após isso, o amálgama de sódio Na(Hg) migra para a câmara secundária onde entra em contato com água, nesse momento o mercúrio age como anodo oxidando o sódio e transformando-o no cátion sódio (esquema 2), ao mesmo tempo que isso ocorre, a água sofre redução promovendo a formação de gás hidrogênio e fornecendo hidroxilas para reagir com o cátion sódio formando o hidróxido de sódio, observe as reações no esquema 2.
Apesar de ainda ser utilizado na atualidade, esse processo apresenta alto consumo energético e provoca grandes contaminações ao meio ambiente devido ao efluente líquido proveniente da lavagem das células que contém mercúrio. Por esse motivo outros métodos estão sendo empregados na produção de hidróxido de sódio.
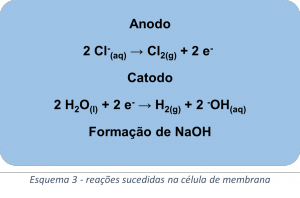
O método da célula de membrana utiliza dois compartimentos separados por uma membrana polimérica de politetrafluoretileno (Imagem 2), o primeiro possui uma entrada para a solução de cloreto de sódio e um anodo, neste compartimento o cloreto sofre oxidação formando gás cloro, observe o esquema 3. Enquanto isso o cátion sódio atravessa a membrana polimérica, que é impermeável ao ânion cloreto, e flui para o segundo compartimento. Neste, a água sofre redução no catodo liberando gás hidrogênio e fornecendo íons hidroxilas que reagem com o sódio iônico proveniente do primeiro compartimento, o resultado desse processo é a formação de hidróxido de sódio, observe o esquema 3.
Diferente das células de Mercúrio esse método não apresenta desvantagens consideráveis, além de econômico ele produz hidróxido de sódio com alto grau de pureza.
O método da célula de diafragma funciona da mesma forma que a célula de membrana, porém ao invés de usar uma membrana polimérica ele utiliza um diafragma que só permite a migração do cátion sódio para o segundo compartimento. Apesar de ser energeticamente mais econômico que a célula de mercúrio, o diafragma é feito de amianto, um material que gera resíduos indestrutíveis que podem causar câncer aos trabalhadores que lidam com o processo de fabricação do hidróxido de sódio, em razão disso, nas últimas décadas, as empresas tentam substituir esse pela membrana polimérica da célula de membrana
Por fim, é importante salientar que as empresas estão em constante busca de aprimoramento, por isso pesquisas voltadas a redução do consumo energético das células e a diminuição da quantidade de efluente liberado estão sendo realizadas.
Bibliografia:
Lakshmanan, Shyam, and Thanapalan Murugesan. “The chlor-alkali process: work in progress.” Clean Technologies and Environmental Policy 16.2 (2014): 225-234.
da Silva, Illana MCB. “Hidróxido de Sódio (CAS Nº 1310-73-2).” Revista Virtual de Química 4.1 (2012): 73-82.